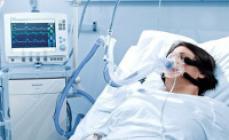
Введение
Разделение и очистка веществ являются операциями, обычно связанными между собой. Разделение смеси на составляющие чаще всего преследует цель получения чистых, по возможности без примесей, веществ. Однако само понятие о том, какое вещество следует считать чистым, еще окончательно не установлено, так как требования к чистоте вещества меняются. В настоящее время методы получения химически чистых веществ приобрели особое значение.
Разделение и очистка веществ от примесей основываются на использовании их определенных физических, физико-химических или химических свойств.
Техника важнейших методов разделения и очистки веществ (перегонка и сублимация, экстракция, кристаллизация и перекристаллизация, высаливание) описана в соответствующих главах. Это -- наиболее распространенные приемы, чаще всего используемые не только в лабораторной практике, но и в технике.
В отдельных наиболее сложных случаях используют специальные методы очистки.
Очистка веществ
Перекристаллизация
Очистка перекристаллизацией основана на изменении растворимости вещества с изменением температуры.
Под растворимостью понимают содержание (концентрацию) растворенного вещества в насыщенном растворе. Она обычно выражается или в процентах, или в граммах растворенного вещества на 100 г растворителя.
Растворимость вещества зависит от температуры. Эта зависимость характеризуется кривыми растворимости. Данные о растворимости некоторых веществ в воде приведены на рис. 1, а также в таблице растворимости.
Согласно этим данным, если, например, приготовить раствор нитрата калия, взяв 100 г воды, насыщенный при 45є, а затем охладить его до 0є, то должно выпасть 60 г кристаллов KNO 3 . Если соль содержала малые количества других растворимых в воде веществ, насыщение относительно их не будет достигнуто при указанном понижении температуры, а потому они и не выпадут вместе с кристаллами соли. Ничтожные количества примесей, часто не поддающиеся определению обычными методами анализа, могут лишь увлекаться кристаллами осадка. Однако при повторных перекристаллизациях можно получить практически чистое вещество.
Насыщенный раствор соли, который остается после отфильтрования выпавших кристаллов, тем более чистыми они получаются, так как в этом случае они меньше захватывают маточного раствора, содержащего примеси других веществ. Уменьшению примесей содействует промывание кристаллов растворителем после отделения их от маточного раствора.
Таким образом, перекристаллизация сводится к растворению вещества в подходящем растворителе и последующему выделению его из образовавшегося раствора в виде кристаллов. Это один из распространенных методов очистки веществ от примесей.
Возгонка
Возгонкой, или сублимацией, называется непосредственное превращение твердого вещества в пар без образования жидкости. Достигнув температуры возгонки, твердое вещество без плавления переходит в пар, который конденсируется в кристаллы на поверхности охлажденных предметов. Возгонка всегда происходит при температуре ниже температуры плавления вещества.
Используя свойство ряда веществ (йода, нафталина, бензойной кислоты, нашатыря и др.) возгоняться, легко получить в чистом виде, если примесь лишена этого свойства.
Для более глубокого изучения явления возгонки необходимо познакомится с диаграммой состояния вещества, представленной на рис. 2. На оси абсцисс отложена температура t (в градусах Цельсия) на оси ординат - давление насыщенного пара p (в м/см 3). Аналогичный вид имеет диаграмма состояния воды, так что у нее кривая ТВ наклонена к оси ординат, так как температура замерзания воды по мере возрастания давления понижается.
Кривая ТА выражает зависимость между температурой и давлением насыщенного пара над жидкостью. Все точки кривой ТА определяют условия равновесия между жидкостью и ее насыщенным паром. Например, при 100є вода и пар могут существовать только при давлении 760 мм рт. ст. Если давление больше 760 мм рт. ст., то пар конденсируется в воду (область выше кривой ТА); если давление меньше 760 мм рт. ст., то вся жидкость превращается в пар (область ниже кривой ТА). Кривая ТА лежит выше температуры плавления вещества. Кривая ТБ выражает зависимость между температурой и давлением насыщенного пара над твердым телом. Давление пара твердых тел обычно невелико и в значительной степени зависит от природы тела и температуры. Так, давление паров йода при 16є равно 0,15 мм рт. ст., льда при - 15є равно 1,24 мм рт. ст. Кривая ТБ лежит ниже температуры плавления вещества. Все точки этой кривой определяют условия равновесия между твердым телом и его насыщенным паром.
Кривая ТВ называется кривой плавления и выражает зависимость между температурой плавления вещества и давлением.
Все точки этой кривой определяют условия (температуру и давление), при которых твердое вещество и жидкость находятся в равновесии.
Кривые ТА, ТБ и ТВ разделяют диаграмму состояния вещества на три области: 1 - область существования твердой фазы, 2 - жидкой фазы и 3 - парообразной фазы.
Точка Т, где сходятся все три области, указывает температуру и давление, при которых могут находится в равновесии все три фазы вещества - твердая, жидкая и парообразная. Она называется тройной точкой (Т).
Изменяя температуру или давление, можно изменять состояние вещества.
Пусть точка 1 изображает твердое состояние вещества при давлении выше тройной точки. При нагревании вещества при постоянном давлении точка 1 будет двигаться по пунктирной линии 1-4 и при определенной температуре пересечет кривую плавления ТВ в точке 2. Когда все кристаллы расплавятся, дальнейшее нагревание при постоянном давлении приведет в точку 3 на кривой ТА, где начинается кипение жидкости, вещество перейдет в парообразное состояние. При дальнейшем увеличении температуры тело из состояния 3 перейдет в состояние 4. Охлаждение пара повторит рассмотренные процессы в обратном направлении по той же пунктирной кривой из состояния 4 в состояние 1.
Если взять вещество при давлении ниже тройной точки, например в точке 5, то, нагревая вещество при постоянном давлении, достигнем точки 6, в которой твердое вещество будет переходить в пар без предварительного образования жидкости, т.е. будет иметь место возгонка или сублимация (см. пунктирную линию 5-7). Наоборот, при охлаждении пара при томжелавлении произойдет в точке 6 кристаллизация вещества (также без образования жидкости).
Из изложенного можно сделать следующие выводы:
1) В результате нагревания твердого вещества при давлении выше тройной точки оно будет плавиться;
2) В результате нагревания твердого вещества при давлении ниже тройной точки оно будет возгоняться;
3) Если произвести нагревание при атмосферном давлении, то возгонка наступит в том случае, если давление тройной точки данного вещества выше атмосферного. Так, например, при р=1 ат двуокись углерода возгоняется при - 79є, плавиться же будет при условии, что нагревание проводится при давлении более высоком, чем давление тройной точки.
Следует иметь в виду, что твердые вещества могут переходить в пар при давлении выше тройной точки (поскольку все тверды тела и жидкости частично испаряются при всякой температуре). Так, кристаллический йод при атмосферном давлении ниже температуры плавления переходит в пар фиолетовго цвета, который легко конденсируется в кристаллы на холодной поверхности. Это свойство используют для очистки йода. Однако поскольку давление тройной точки у йода ниже атмосферного, то при дальнейшем нагревании он будет плавиться. Поэтомукристаллический йод при атмосферном давлении не может находится в равновесии со своим насыщенным паром.
В равновесии со своим насыщенным паром могут быть лишь твердые вещества, которые находятся под давлением ниже тройной точки. Но пр таком давлении эти вещества не могут плавиться. Возгоняемые вещества можно перевести в жидкое состояние путем нагревания их при определенном давлении.
Для проведения анализа вещества его сначала надо выделить, т.е. очистить, т.к. свойства вещества зависят от его чистоты. При выделении вещества из смеси веществ часто используют их различную растворимость в воде или органических растворителях.
Перекристаллизация – очистка твердых веществ, основанная на увеличении растворимости твердых веществ при повышении температуры в данном растворителе. Вещество растворяют в дистиллированной воде или подходящем органическом растворителе при определенной повышенной температуре. В горячий растворитель небольшими порциями вводят кристаллическое вещество до тех пор, пока оно перестанет растворяться, т.е. образуется насыщенный при данной температуре раствор. Горячий раствор отфильтровывают на воронке для горячего фильтрования через бумажный фильтр или, если растворитель агрессивная жидкость через фильтр Шотта (воронки с впаянной пористой стеклянной пластинкой). При этом раствор освобохдается от взвешенных мелких твердых частиц.
Фильтрат собирают в стакан, поставленный в кристаллизатор с холодной водой со льдом или с охлаждающей смесью. При охлаждении из отфильтрованного насыщенного раствора выпадают мелкие кристаллы растворенного вещества, т.к. раствор при более низкой температуре становится пересыщенным. Выпавшие кристаллы отфильтровывают на воронке Бюхнера. Для ускорения фильтрования и более полного освобождения осадка от раствора используют фильтрование под вакуумом. Для этой цели собирают прибор для фильтрования под вакуумом (рис. 15.1). Он состоит из колбы Бунзена (1), фарфоровой воронки Бюхнера (2), предохранительной склянки (4) и водоструйного вакуум-насоса(10). При этом в фильтрат уходят растворимые примеси, которые не кристаллизуются вместе с основным веществом, т.к. раствор не был пересыщен относительно примесей.
Рис. 15.1. Установка для фильтрования под вакуумом. 1 – колба Бунзена, 2 – воронка Бюхнера, 3 – пробка резиновая с отверстием, 4 – колба, 5 – кран соединительный, 6 – труба стеклянная газоотводная, 7 – пробка резиновая с тремя отверстиями, 8, 11 – шланг резиновый, 9 – шланг ПВХ, 10 – насос водоструйный
Отфильтрованные кристаллы вместе с фильтром из воронки Бюхнера переносят на сложенный вдвое лист фильтровальной бумаги и отжимают между листами фильтровальной бумаги. Операцию повторяю несколько раз, затем кристаллы переносят в бюкс. До постоянной массы вещество доводят в электрическом сушильном шкафу при температуре 100–105°С.
Возгонка – метод применяется для очистки веществ, способных при нагревании переходить из твердого состояния в газообразное, минуя жидкое состояние. Далее пары очищаемого вещества конденсируются, а примеси, не способные возгоняться, отделяются. Легко возгоняются такие вещества, как кристаллический иод, хлорид аммония (нашатырь), нафталин. Однако этот метод очистки веществ ограничен, т.к. немногие твердые вещества способны сублимироваться.
Разделение двух несмешивающихся жидкостей, имеющих различную плотность и не образующих устойчивых эмульсий, можно осуществить с помощью делительной воронки (рис. 15.2). Так можно разделить, например, смесь бензола и воды. Слой бензола (плотность r = 0,879 г/см 3) располагается над слоем воды, которая имеет большую плотность (r = 1,0 г/см 3). Открыв кран делительной воронки, можно аккуратно слить нижний слой и отделить одну жидкость от другой.

Рис. 15.2. Делительная воронока .
Для разделения жидких веществ (чаще всего органических) используется их растворимость в несмешивающихся растворителях. После отстаивания в делительной воронке слои растворителей разделяют, поочередно сливая. Потом растворитель выпаривают или отгоняют. Для очистки органических веществ часто применяют различные виды перегонки: фракционную, с водяным паром, под низким давлением (в вакууме).
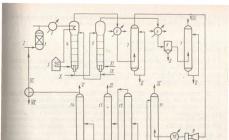
Фракционная перегонка (рис. 15.3)применяется для разделения смесей жидкостей с различными температурами кипения. Жидкость с меньшей температурой кипения закипает быстрее и раньше проходит через фракционную колонку (или дефлегматор ). Когда эта жидкость достигает верха фракционной колонки, то попадает в холодильник , охлаждается водой и через аллонж собирается в приемник (колбу или пробирку).

Рис. 15.3 Установка для фракционной перегонки: 1 – термометр; 2 – дефлегматор; 3 – холодильник; 4 – алонж; 5 – приемник; 6 – перегонная колба; 7 – капилляры; 8 – нагреватель.
Фракционной перегонкой можно разделить, например, смесь этанола и воды. Температура кипения этанола 78°С, а воды 100°С. Этанол испаряется легче и первым попадает через холодильник в приемник.
Хроматография (адсорбционная) – метод разделения смесей, предложенный в 1903 г М.С. Цветом. Являясь общепризнанным физико-химическим методом, хроматография позволяет разделять, а также проводить качественный и количественный анализ самых разнообразных смесей. В основе хроматографических методов лежит широкий круг физико-химических процессов: адсорбция, распределение, ионный обмен, диффузия и т.д. Разделение анализируемой смеси часто ведут на колонках, наполненных силикагелем, оксидом алюминия, ионитами (ионообменными смолами) или же на специальной бумаге. Вследствие различной сорбируемости определяемых компонентов смеси (подвижная фаза) происходит их зональное распределение по слою сорбента (неподвижная фаза) – возникает хроматограмма, позволяющая выделить и проанализировать индивидуальные вещества.
После очистки соединения можно приступать к качественному анализу. Для определения состава органического вещества устанавливают, какие элементы входят в его состав. Для этого элементы из состава этого вещества переводят в хорошо известные неорганические вещества и открывают их методами неорганической и аналитической химии.
Очистка растворимых солей методом перекристаллизации . Метод перекристаллизации основан на различной зависимости растворимости веществ и загрязняющих его примесей от температуры. Очистку вещества методом перекристаллизации проводят по следующей схеме: при повышенной температуре готовят насыщенный раствор очищаемого вещества, затем для удаления нерастворимых примесей раствор фильтруют через воронку для горячего фильтрования и охлаждают до низкой температуры. При понижении температуры растворимость вещества понижается и основная часть очищаемого вещества выпадает в осадок, растворимые примеси остаются в растворе, поскольку относительно них раствор остается ненасыщенным. Выпавшие кристаллы отделяют от маточного раствора и высушивают.
В зависимости от свойств очищаемого вещества возможны различные методики проведения перекристаллизации.
Перекристаллизация без удаления растворителя . Метод применяется для солей, растворимость которых сильно зависит от температуры (например, нитрат натрия, алюмокалиевые квасцы, сульфат меди (II) и др.). Раствор после горячего фильтрования охлаждают на воздухе до низкой температуры, выпавшие кристаллы отфильтровывают. Возможно также провести перекристаллизацию без удаления растворителя для солей, растворимость которых мало зависит от температуры. В этом случае применяется метод высаливания. Для этого раствор после горячего фильтрования охлаждают до комнатной температуры и добавляют равный по объему раствор концентрированной соляной кислоты, при этом очищаемое вещество выпадает в осадок.
Перекристаллизация с удалением растворителя . Метод применяется для солей, растворимость которых мало зависит от температуры (например, хлорид натрия и др.). Раствор после горячего фильтрования переносят во взвешенную фарфоровую чашку и упаривают на водяной бане приблизительно до половины объема. Затем раствор охлаждают до комнатной температуры. Выпавшие кристаллы отфильтровывают.
Перекристаллизованное вещество (за исключением хлорида аммония и кристаллогидратов) сушат в сушильном шкафу до постоянной массы. Хлорид аммония и кристаллогидраты высушивают на воздухе. Сухие соли помещают в герметичные склянки.
Очистка летучих веществ методом сублимации (возгонки) . Метод применяется для очистки твердых веществ, способных при нагревании переходить непосредственно из твердой фазы в газообразную, минуя жидкую фазу. Образующийся газ конденсируется охлаждаемой частью прибора. Сублимацию обычно проводят при температуре, близкой к температуре плавления вещества. Метод применим для очистки от примесей, которые не способны возгоняться. Возгонкой можно очистить йод, серу, хлорид аммония.
Очистка жидкостей методом перегонки . Метод основан на том, что каждое вещество имеет определенную температуру кипения. Наиболее простой вариант перегонки - перегонка при обычном давлении, который заключается в нагревании жидкости до кипения и конденсации её паров. Перегонку проводят в приборе, состоящем из колбы Вюрца (или круглодонной колбы с газоотводной трубкой), прямого холодильника, колбы-приемника, аллонжа, термометра и нагревательного прибора. Загрязненную жидкость нагревают в перегонной колбе до температуры кипения, пары отводят в холодильник и собирают сконденсировавшуюся жидкость в приемник.
Введение
Бор в основном применяется в виде буры.
БУРА - натриевая соль тетраборной кислоты. Она широко применяется при производстве легкоплавкой глазури для фаянсовых и фарфоровых изделий и, особенно для чугунной посуды (эмаль); кроме того, она идет для приготовления специальных сортов стекла.
На растворении окислов металлов основано применение буры при спаивании металлов. Так как можно спаивать только чистые поверхности металлов, то для удаления окислов место спайки посыпают бурой, кладут на него припой и нагревают. Бура растворяет окислы, и припой хорошо пристает к поверхности металла.
Бор играет важную роль в жизни растений. присутствие в почве небольшого количества соединений бора необходимо для нормального роста с/х культур, как, например хлопка, табака, сахарного тростника и др.
В ядерной технике бор и его сплавы, а также карбид бора применяют для изготовления стержней реакторов. Бор и его соединения используют в качестве материалов, защищающих от нейтронного излучения.
Данная работа посвящена методам очистки буры как основного вещества – источника бора.
Бура и ее свойства
Тетрабора́т на́трия («бура») - Na 2 B 4 O 7 , соль слабой борной кислоты и сильного основания, распространённое соединение бора, имеет несколько кристаллогидратов, широко применяется в технике.
Химия
Структура аниона 2− в буре
Термин «бура» применяют по отношению к нескольким близким веществам: она может существовать в безводной форме, в природе чаще встречается в виде пятиводного или десятиводного кристаллогидрата:
· Безводная бура (Na 2 B 4 O 7)
· Пентагидрат (Na 2 B 4 O 7 ·5H 2 O)
· Декагидрат (Na 2 B 4 O 7 ·10H 2 O)
Однако наиболее часто слово бура относят к соединению Na 2 B 4 O 7 ·10H 2 O.
Природные источники

Бура, «cottonball»
Тетраборат натрия (Бура) встречается в солевых отложениях, образованных при испарении сезонных озёр.
Бура́ (декагидрат тетрабората натрия, Na 2 B 4 O 7 · 10H 2 O) - прозрачные кристаллы, при нагревании до 400°C полностью теряют воду.
Обычная бура (десятиводный гидрат) образует большие бесцветные прозрачные призматические кристаллы; базоцентрированная моноклинная решётка, а = 12, 19 Å, b = 10, 74 Å, с = 11, 89 Å, ß = 106°35´; плотностью 1, 69 - 1, 72 г/см 3 ; в сухом воздухе кристаллы выветриваются с поверхности и мутнеют.
В воде бура гидролизуется, её водный раствор имеет щелочную реакцию.
С оксидами многих металлов бура при нагревании образует окрашенные соединения - бораты («перлы буры»). В природе встречается в виде минерала тинкаля.
Тинкал, или «Бура» (декагидрат тетрабората натрия, Na 2 B 4 O 7 ·10H 2 O) - минерал моноклинной сингонии, призматический. «Тинкал» (Tinkal) - слово санскритского происхождения, являющееся синонимом более часто употребляемого названия минерала - «Бура» (от арабского «бюрак» - белый).
Цвет белый, блеск стеклянный, твёрдость по Моосу 2 - 2,5.
Плотность 1,71.
Спайность средняя по (100) и (110).
Образует короткопризматические кристаллы, по форме напоминающие кристаллы пироксенов, а также сплошные зернистые массы и прожилки в глинистых породах.
Типичный минерал эвапоритов.
На воздухе разрушается, теряя кристаллизационную воду и покрывается коркой тинкалконита или кернита, со временем превращается в них полностью.
Так называемая Ювелирная бура - пятиводный тетраборат натрия Na 2 B 4 O 7 ·5H 2 O.
Бура применяется:
· в производстве эмалей, глазурей, оптических и цветных стекол;
· при пайке и плавке в качестве флюса;
· в бумажной и фармацевтической промышленности;
· в производстве строительных материалов как компонент антисептика для изготовления целлюлозного утеплителя «Эковата»
· как дезинфицирующее и консервирующее средство;
· в аналитической химии:
o как стандартное вещество для определения концентрации растворов кислот;
o для качественного определения оксидов металлов (по цвету перлов);
· в фотографии - в составе медленно действующих проявителей в качестве слабого ускоряющего вещества;
· как компонент моющих средств;
· как компонент косметики;
· как сырьё для получения бора;
· как инсектицид в отравленных приманках для уничтожения тараканов.
В сухом воздухе кристаллы выветриваются с поверхности и мутнеют. При нагревании до 80°С декагидрат теряет 8 молекул воды, при 100 градусах медленно, а при 200°С быстро отщепляется ещё одна молекула воды, в интервале 350 - 400°С происходит полное обезвоживание.
Растворимость буры (в г. безводной соли на 100 г. воды): 1, 6 (10°С), 3, 9 (30°С), 10, 5 (50°С). Насыщенный раствор кипит при 105°С.
В воде бура гидролизуется, поэтому её раствор имеет щелочную реакцию.
Щелочная реакция раствора тетрабората натрия обусловлена тем, что в водном растворе протекает реакция гидролиза c образованием в растворе борной кислоты B(OH) 3:
Na 2 B 4 O 7 = 2Na + + B 4 O 7 2– ;
B 4 O 7 2– + 7H 2 O 2OH – + 4B(OH) 3 ,
а выделение аммиака при взаимодействии с NH4Cl отвечает уравнению:
Na 2 B 4 O 7 + 2NH 4 Cl + H 2 O = 2NH 3 + 2NaCl + 4B(OH) 3
Бура растворяется в спирте и глицерине.
Сильными кислотами полностью разлагается:
Na 2 B 4 O 7 + H 2 SO 4 + 5H 2 O = Na 2 SO 4 + 4H 3 BO 3 .
Именно так голландский алхимик Вильгельм Гомберг, нагревая буру с серной кислотой H 2 SO 4 , выделил борную кислоту B(OH) 3 .
С окислами некоторых металлов бура даёт окрашенные бораты («перлы буры»):
Na 2 B 4 O 7 + CoO = 2NaBO 2 + Co(BO 2) 2 ,
что используется в аналитической химии для открытия этих металлов.
При медленном охлаждении раствора обычной буры при 79°С начинает выкристаллизовываться октаэдрическая бура Na 2 B 4 O 7 . 5H 2 O (или «ювелирная бура»), плотностью 1, 815 г/см 3 , устойчивая в интервале 60 - 150°С. Растворимость этой буры составляет 22 г. в 100 г. воды при 65°С, 31, 4 при 80°С и 52, 3 при 100°С.
Бура является важнейшим флюсом, облегчающим процесс плавки. Расплавленная бура образует при охлаждении на стенках тигля глазурь, предохраняет расплав от доступа кислорода и растворяет окислы металлов.
При медленном термическом обезвоживании обычной буры получается пиробура с плотностью 2, 371 г/см 3 и температурой плавления 741°С. Бура плавится и распадается на метаборат натрия и трёхокись бора, которые смешиваются в жидком состоянии:
Na 2 B 4 O 7 → 2NaBO 2 + B 2 O 3 .
Окись бора, соединяясь с окислами металлов, образует метабораты так же, как борная кислота. Метаборат натрия легко смешивается со вновь образованными метаборатами и быстро уводит их из зоны расплавленного металла, а на их место вступают новые активные молекулы окиси бора.
Бура обладает большей способностью растворять окислы, чем борная кислота, и используется не только как плавильный восстановительный флюс, но и как важнейший флюс при пайке твёрдыми припоями.
Обычную буру получают из борной кислоты, из тинкаля, кернита и некоторых других минералов (путём их перекристаллизации), а также из воды соляных озёр (фракционированной кристаллизацией).
Буру широко применяют при приготовлении эмалей, глазурей, в производстве оптических и цветных стёкол, при сварке, резке и пайке металлов, в металлургии, гальванотехнике, красильном деле, бумажном, фармацевтическом, кожевенном производствах, в качестве дезинфицирующего и консервирующего средства и удобрения.
Очистка веществ методом перекристаллизации
Перекристаллиза́ция - метод очистки вещества, основанный на различии растворимости вещества в растворителе при различных температурах (обычно интервал температур от комнатной до температуры кипения растворителя, если растворитель - вода, или до какой-то более высокой температуры).
Перекристаллизация подразумевает плохую растворимость вещества в растворителе при низких температурах, и хорошую - при высоких. При нагревании колбы вещество растворяется. После стадии адсорбции примесей (если это необходимо) активированным углём, горячего фильтрования (при необходимости) и охлаждения образуется перенасыщенный раствор, из которого растворённое вещество выпадает в виде осадка. После пропуска смеси через колбу Бунзена и воронку Бюхнера либо центрифугирования получаем очищенное растворённое вещество.
· Достоинство метода: высокая степень очистки.
· Недостаток метода: сильные потери вещества в ходе перекристаллизации: всегда часть растворённого вещества в осадок не выпадет, потери при перекристаллизации нередко составляют 40-50 %.
Растворителем могут быть вода, уксусная кислота, этанол (95 %), метанол, ацетон, гексан, пентан - в зависимости от условий.
Если растворителем является вода, то нагревание проводят в водяной бане. Охлаждение перенасыщенного раствора проводят с помощью водяного холодильника, если температура кипения растворителя ниже 130 градусов, если выше - с помощью воздушного холодильника.
Растворимость большинства твердых веществ с ростом температуры увеличивается. Если приготовить горячий концентрированный (почти насыщенный) раствор такого вещества, то при охлаждении этого раствора начнется выпадение кристаллов, поскольку растворимость вещества при более низкой температуре меньше. Образование холодного насыщенного раствора, концентрация которого меньше, чем исходного (горячего), будет сопровождаться кристаллизацией «излишка» вещества.
Растворение вещества, содержащего растворимые примеси, в горячей воде, а затем осаждение его из раствора при достаточном охлаждении - это способ очистки вещества от растворимых примесей, который называют перекристаллизацией. Примеси при этом, как правило, остаются в растворе, так как присутствуют там в ничтожно малых («следовых») количествах и при охлаждении не могут образовать своего насыщенного раствора.
Некоторая часть очищаемого вещества также остается в холодном насыщенном растворе, который в лабораторной практике называют маточным , и такие неизбежные (плановые) потери вещества можно рассчитать по значению растворимости вещества при этой температуре.
Чем больше уменьшается растворимость вещества при охлаждении раствора, тем выше будет выход перекристаллизованного вещества.
Многие твердые вещества при кристаллизации из водного раствора образуют кристаллогидраты; например, из водного раствора сульфат меди (II) кристаллизуется в виде CuSO 4 ·5 H 2 O. В этом случае при расчете необходимо учитывать воду, которая входит в состав кристаллогидрата.
Перекристаллизация имеет большое значение в химии и химической технологии, поскольку подавляющее большинство твердых веществ - химических продуктов, реактивов, химикатов, лекарств и т.д. получают из водных и неводных растворов, а заключительная стадия этого получения - кристаллизация (или перекристаллизация с целью повышения чистоты продукта). Поэтому очень важно проводить указанные процессы эффективно, с наименьшими потерями и высокими показателями качества.
Для проведения перекристаллизации используют специальную химическую посуду и лабораторное оборудование.
Процесс перекристаллизации осуществляют в несколько стадий:
Выбор растворителя;
Приготовление насыщенного горячего раствора;
- «Горячая» фильтрации;
Охлаждение раствора;
Отделение образовавшихся кристаллов;
Промывание кристаллов чистым растворителем;
Высушивание.
Выбор растворителя
Правильный выбор растворителя - условие при проведении перекристаллизации.
К растворителя выдвигают ряд требований:
Значительная разница между растворимостью вещества в определенном растворителе при комнатной температуре и при нагревании;
Растворитель должен растворять при нагревании только вещество и не растворять примеси. Эффективность перекристаллизации возрастает при увеличении разности в растворимости вещества и примесей;
Растворитель должен быть индифферентным как к веществу, так и к примесям;
Температура кипения растворителя должна быть ниже температуры плавления вещества на 10 - 15°С, иначе при охлаждении раствора вещество выделится не во кристаллической форме, а в виде масла.
Экспериментально растворитель выбирают так: небольшую пробу вещества помещают в пробирку, добавляя в нее несколько капель растворителя. Если вещество растворяется без нагревания, такой растворитель не пригоден для перекристаллизации.
Выбор растворителя считается правильным, если вещество плохо растворяется в нем без нагрева, хорошо - при кипении, а при охлаждении горячего раствора происходит ее кристаллизация.
Как растворитель при перекристаллизации используют воду, спирты, бензол, толуол, ацетон, хлороформ и другие органические растворители или их смеси.
Вещество для перекристаллизации помещают в колбу (1), добавляют небольшую порцию растворителя и нагревают с обратным холодильником (2) до кипения раствора. Если исходного количества растворителя не хватает для полного растворения вещества, растворитель небольшими порциями добавляют с помощью воронки через обратный холодильник.
Эффективная очистка сильно загрязненных веществ возможно с помощью различных адсорбентов (активированный уголь (activeated carbon), силикагель и т.д.). В этом случае готовят горячий насыщенный раствор вещества, охлаждают его до 40 - 50°С, добавляют адсорбент (0,5 – 2 % от массы вещества) и снова кипятят с обратным холодильником в течение нескольких минут.
«Горячая» фильтрация
Для отделения от механических примесей и адсорбента горячий раствор фильтруют. Чтобы предотвратить выделение вещества на фильтре применяют различные методы.
Простая установка «горячего» фильтрования (рис. 3.2) состоит из специальной воронки для «горячего» фильтрования (1), обогреваемой паром, химической воронки (2) со складчатым фильтром (3), который помещается в нее.
Горячий насыщенный раствор вещества быстро выливают на бумажный фильтр, помещенный в стеклянную воронку, которая нагревается с помощью воронки для горячего фильтрования. Фильтрат собирают в стакан или коническую колбу. При образовании на фильтре кристаллов вещества их промывают небольшим количеством горячего растворителя.
Охлаждение раствора
При охлаждении фильтрата до комнатной температуры начинается процесс кристаллизации. Для ее ускорения фильтрат охлаждают под струей холодной воды. При этом растворимость вещества уменьшается, происходит окончательная кристаллизация.
Отделение образовавшихся кристаллов
Отделение кристаллов от растворителя осуществляют с помощью фильтрования, при этом отсос или создания вакуума в приемнике часто используют для ускорения процесса фильтрования. Для этого используют вакуумный насос (водоструйный, масляный или Камовского).
Фильтрация осуществляется на установке, которая состоит из воронки Бюхнера (1) с бумажным фильтром, колбы Бунзена или специальной пробирки (2), промежуточной стакана (3) и вакуумного насоса. Размер бумажного фильтра должен точно совпадать с площадью дна воронки Бюхнера.
Бумажный фильтр смачивают растворителем, вкладывают в воронку и включают вакуумный насос. При работе насоса под фильтром создается пониженное давление - возникает характерный звук, что свидетельствует о наличии вакуума в системе и возможность фильтрации. Охлажденный кристаллический продукт вместе с растворителем при взбалтывании небольшими порциями переносят с конической колбы на бумажный фильтр.
В процессе фильтрования растворитель проходит через фильтр, осадок остается на нем. Следует следить, чтобы фильтрат НЕ заполнил колбу до уровня тубуса, соединенного с промежуточной стаканом. Фильтрация продолжают до тех пор, пока не перестанет капать фильтрат. После этого осадок отжимают на фильтре широкой стеклянной пробкой или специальной стеклянной палочкой, выключают насос, промывают осадок чистым растворителем, включают насос и снова отжимают. Установку отсоединяют от вакуума, вынимают воронку. Фильтр вместе с веществом аккуратно переносят в чашку Петри или специальную емкость для высушивания.
Высушивание твердого вещества
Сушить твердое вещество можно на воздухе при комнатной температуре. Гигроскопичны вещества высушивают в эксикаторах; устойчивы к воздействию воздуха и температуры - в сушильном шкафу, где температура должна быть на 20 - 50°С ниже температуры плавления данного вещества. Для перекристаллизованного и высушенного продукта определяют массу, выход и температуру плавления.
Определение температуры плавления
Температурой плавления вещества считают температурный интервал от начала до полного расплавления этого вещества. Чем чище вещество, тем меньше этот интервал. Разница между температурой, при которой начинается образование жидкой фазы и температурой полного расплавления для чистых соединений, не превышает 0,5°С.
Наличие незначительного количества примесей в веществе снижает ее температуру плавления и соответственно увеличивает интервал плавления. Это свойство используют для установления идентичности двух веществ, если одна из них известна: тщательно смешивают одинаковые количества веществ и определяют температуру плавления смеси (смешанная проба). Если температура плавления смешанной пробы такая же, как и у чистого вещества, делают вывод об идентичности обоих веществ.
Температуру плавления кристаллической органического вещества определяют в капилляре. Капилляр извлекают из стеклянной трубки, нагревая ее на пламени горелки. Один конец капилляра запаивают.
Перекристаллизованное вещество тщательно растирают на часовом стекле или в ступке. Открытым концом капилляра набирают небольшое количество вещества и бросают его запаянным концом вниз в стеклянную трубку длиной ≈ 60 - 80 см, поставленную вертикально на лабораторный стол. Операцию наполнения капилляра повторяют несколько раз, пока в нем не образуется цельный столбик вещества высотой 2 - 3 мм.
Наполненный капилляр (1) закрепляют резиновыми кольцами (2) на термометре (3) так, чтобы проба вещества находилась на уровне шарики термометра. Нагрев прибора регулируют так, чтобы температура увеличивалась со скоростью 1°С в минуту. При этом внимательно следят за состоянием колонки вещества капилляре, отмечая все изменения - изменение окраски, разложение, спекание, намокания и т.п.. Началом плавления считают возникновение первой капли в капилляре (Т 1), а окончанием - окончание расплавления последних кристалликов вещества (Т 2). Интервал температур (Т 2 - Т 1) называют температурой плавления данного вещества (Т пл).
Практическая часть
Методики очистки
1 способ. 25 г буры при 60 0 С растворяют в 50 мл воды. Раствор быстро фильтруют через складчатый фильтр в фарфоровую чашку или стакан, охлаждаемый снегом. Фильтрат непрерывно помешивают стеклянной палочкой.
Тетраборат натрия выпадает в виде мелких кристаллов, их отсасывают, промывают небольшим количеством холодной воды и повторяют перекристаллизацию. Кристаллы высушивают на воздухе в течение 2 – 3 дней. Полученный препарат имеет формулу Na 2 B 4 O 7 *10H 2 O и пригоден для установки титра.
2 способ. 25 г буры при 65 - 70 0 С растворяют в 75 мл воды. Полученный раствор быстро фильтруют через складчатый фильтр, вставленный в воронку с обрезанным концом, или через воронку для горячего фильтрования. Фильтрат сначала охлаждают медленно до 25 - 30 0 С, а затем быстро в ледяной воде или в снегу, усиливая кристаллизацию перемешиванием палочкой. Выпавшие кристаллы отсасывают, промывают небольшим количеством ледяной воды и высушивают между листами фильтровальной бумаги в течение 2 – 3 дней. Высушенные кристаллы буры должны легко отставать от сухой палочки.
Рассчитывают процент практического выхода буры.
Перекристаллизованную буру хранят в банке с хорошо притертой пробкой.
Дополнительный материал для учителя
8 класс по теме «Очистка веществ»
Аннотация
В предлагаемом дополнительном материале дано описание специальных методов очистки: диализ, комплексообразование, образование летучих соединений, хроматография и ионный обмен, дистилляция и ректификация, экстракция, зонная плавка.
Разделение и очистка веществ являются операциями, обычно связанными между собой. Разделение смеси на составляющие чаще всего преследует цель получения чистых, по возможности без примесей, веществ. Однако само понятие о том, какое вещество следует считать чистым, еще окончательно не установлено, так как требования к чистоте вещества меняются. В настоящее время методы получения химически чистых веществ приобрели особое значение.
Разделение и очистка веществ от примесей основываются на использовании их определенных физических, физико-химических или химических свойств.
Техника важнейших методов разделения и очистки веществ (перегонка и сублимация, экстракция, кристаллизация и перекристаллизация, высаливание) описана в соответствующих главах. Это наиболее распространенные приемы, чаще всего используемые не только в лабораторной практике, но и в технике.
В отдельных наиболее сложных случаях используют специальные методы очистки.
Диализ может быть использован для разделения и очистки веществ, растворенных в воде или в органическом растворителе. Этим приемом чаще всего пользуются для очистки высокомолекулярных веществ, растворенных в воде, от примесей низкомолекулярных или от неорганических солей.
Для очистки методом диализа необходимы так называемые полупроницаемые перегородки, или «мембраны» Особенность их заключается в том, что они имеют поры, позволяющие проходить через них веществам, размер молекул или ионов которых меньше размеров пор, и задерживать вещества, размеры молекул или ионов которых больше размеров пор мембраны. Таким образом, диализ можно рассматривать как особый случай фильтрования.
В качестве полупроницаемых перегородок или мембран могут быть использованы пленки из очень многих высокомолекулярных и высокополимерных веществ. В качестве мембран применяют пленки из желатина, из альбумина, пергамент, пленки из гидратцеллюлозы (типа целлофана), из эфиров целлюлозы (ацетат, нитрат и др.), из многих продуктов полимеризации и конденсации. Из неорганических веществ находят применение: неглазурованный фарфор, плитки из некоторых сортов обожженной глины (типа коллоидных глин, как бентонит), прессованное мелкопористое стекло, керамика и др.
Основными требованиями к мембранам являются: 1) нерастворимость в том растворителе, на котором приготовлен диализируемый раствор; 2) химическая инертность по отношению как к растворителю, так и к растворенным веществам; 3) достаточная механическая прочность.
Многие мембраны способны набухать в воде или другом растворителе, теряя при этом механическую прочность. Набухшая пленка может быть легко повреждена или разрушена. В подобных случаях пленку для диализа изготовляют на какой-нибудь прочной основе, например на ткани, инертной к растворителю (хлопчатобумажная, шелковая, из стекловолокна, из синтетического волокна и др.), или па фильтровальной бумаге. Иногда для придания мембранам механической прочности их укрепляют металлическими сетками (армирование) из соответствующего металла (бронза, платина, серебро и др.).
Для получения различной пористости у мембран из эфиров целлюлозы или из некоторых других высокополимерных веществ в соответствующие лаки вводят различное количество воды. При высыхании лаковой пленки получается мембрана молочного цвета, имеющая заданную пористость. Для диализа применяют приборы называемые диализаторами. Скорость диализа неодинакова для различных веществ и зависит от ряда условий и свойств вещества, которое очищают. Повышение температуры раствора и обновление растворителя способствуют ускорению диализа. Во многих случаях вместо обычного диализа применяют электродиализ. Применение электрического тока при диализе ускоряет процесс и создает ряд других преимуществ.
Осаждение малорастворимых веществ. Этим приемом широко пользуются для аналитических целей, получая осадки, содержащие только какое-нибудь одно, неорганическое или органическое, вещество. Полученный осадок может быть дополнительно очищен. Аппаратура, применяемая для проведения этого метода, зависит от свойств веществ и свойств растворителей.
Комплексообразование является одним из приемов выделения чистых веществ, особенно неорганических. Комплексные соединения могут быть или труднорастворимыми в воде, но легкорастворимыми в органических растворителях, или наоборот. В первом случае осадки обрабатывают, как описано выше. Если же комплексное соединение легко растворяется в воде, его можно извлечь в чистом виде из водного раствора путем экстрагирования подходящим органическим растворителем или же разрушить комплекс тем или иным путем. Приемом комплексообразования можно выделить металлы в очень чистом виде. Это особенно касается редких и рассеянных металлов, которые могут быть выделены в виде комплексов с органическими веществами.
Образование летучих соединений. Этим приемом можно пользоваться в том случае, если образуется летучее соединение только выделяемого вещества, например какого-либо металла. В том случае, если одновременно образуются летучие соединения примесей, этот прием применять не рекомендуется, так как освобождение от летучих примесей может оказаться затруднительным. Во многих случаях образование летучих галогенидов (хлористые или фтористые соединения) некоторых веществ может оказаться очень эффективным как метод очистки, особенно в сочетании с вакуумной перегонкой. Чем ниже температура возгонки или кипения интересующего нас вещества, тем легче его отделить от других и очистить фракционной перегонкой или диффузией. Скорость диффузии газообразных веществ через полупроницаемые перегородки зависит от плотности и молекулярной массы очищаемого вещества и почти обратно пропорциональна им.
Хроматография и ионный обмен. Эти методы основаны на использовании явления сорбции для извлечения веществ, содержащихся в растворах. Метод хроматографии особенно важен для концентрирования веществ, содержание которых в исходном растворе очень мало, а также для получения чистых препаратов. При помощи этого метода были получены редкоземельные элементы высокой чистоты. Многие фармацевтические и органические препараты очищают и получают в чистом виде при помощи этого метода. Почти во всех случаях, когда поставлена задача очистки или отделения какого-либо вещества из смеси, находящейся в растворе, хроматография и ионный обмен могут оказаться надежными методами.
Для ионного обмена применяют так называемые иониты, представляющие собой неорганические или органические адсорбенты (преимущественно смолы разных марок). По своим химическим свойствам они разделяются на следующие группы: катиониты, аниониты и амфолиты. Катиониты обменивают катионы. Аниониты обладают способностью обменивать анионы. Иониты способны к ионному обмену до полного насыщения их поглощаемым ионом.
Перекристаллизация. Из всех методов очистки солей и других твердых электролитов и органических соединений на первое место по применимости следует поставить перекристаллизацию. Это связано как с простотой процесса, так и с его эффективностью (во всяком случае, при грубой очистке). Воспользовавшись повышением растворимости солей при нагревании, можно приготовить насыщенный при температуре кипения раствор, отфильтровать его от механических примесей и охладить; при этом зачастую удается получить кристаллы достаточно чистой соли. Это связано с тем, что при охлаждении раствор оказывается пересыщенным только по отношению к основному веществу, в то время как примеси, присутствующие в количестве долей процента, остаются в маточном растворе. Такова элементарная схема процесса перекристаллизации. В действительности перекристаллизация протекает гораздо сложнее, так как ей может сопутствовать ряд процессов, значительно снижающих эффективность очистки при кристаллизации. Так, ионы или молекулы примесей могут быть механически захвачены образующимися кристаллами основного вещества (окклюзия, инклюзия). Неизбежна также большая или меньшая адсорбция ионов примесей на поверхности кристаллов, хотя при образовании крупных кристаллов, имеющих небольшую удельную поверхность, роль адсорбции невелика. Образование твердых растворов (изоморфизм) может иметь место в том случае, когда ионы основной соли и ионы примеси отличаются по размерам не более чем на 10-15% и оба вещества кристаллизуются в одинаковой системе. Тогда часть ионов основной соли в процессе роста кристаллов может быть замещена ионами примеси. Может происходить также захват посторонних ионов любого размера, связанный с нарастанием кристалла вокруг адсорбированных ионов. Такие ионы, поскольку они не входят в твердый раствор, представляют собой дефекты кристаллической решетки.
Вполне понятно, что разделение кристаллизацией изоморфных веществ в принципе невозможно. В этих случаях иногда приходится прибегать к особым приемам. Так, при очистке алюмоаммонийных квасцов, предназначенных для изготовления лазерных рубинов, не удается перекристаллизацией избавиться от примеси Fe 3+ , поскольку алюмоаммонийные и железоаммонийные квасцы изоморфны. При рН 2 коэффициент очистки (коэффициентом очистки называется отношение содержания примеси в неочищенном продукте к содержанию примеси в препарате после очистки) не превышает 10. Но если Fe 3+ восстановить до Fe 2+ , то изоморфизм устраняется, и коэффициент очистки доходит до 100. Эффективность очистки вещества перекристаллизацией зависит также от его растворимости. При растворимости вещества, лежащей в пределах 5-30%, очистка происходит значительно полнее, чем при растворимости 75-85%. Отсюда следует, что перекристаллизация нецелесообразна при очистке очень легкорастворимых веществ.
Дистилляция и ректификация. Очистка веществ дистилляцией основана на том, что при испарении смеси жидкостей пар получается обычно иного состава происходит его обогащение легкокипящим компонентом смеси. Поэтому из многих смесей можно удалить легко кипящие примеси или, наоборот, перегнать основное вещество, оставив трудно кипящие примеси в перегонном аппарате. Часто приходится сталкиваться с системами, при перегонке которых все компоненты отгоняются в неизменном соотношении (азеотропные смеси). В этом случае разделения не происходит, и очистка перегонкой невозможна. В качестве примеров азеотропных смесей можно привести водные растворы НСl (20,24% HCl) и этилового спирта (95,57% С 2 Н 5 ОН).
Для получения чистых веществ (особенно при глубокой очистке) вместо простой дистилляции предпочитают использовать ректификацию, т.е. процесс, при котором происходит автоматическое сочетание процессов дистилляции и конденсации. Не вдаваясь в теорию ректификации, укажем лишь, что в ректификационной колонне пар встречается с различными фракциями конденсата, при этом часть менее летучего компонента конденсируется из пара в жидкость, а часть более летучего компонента переходит из жидкости в пар. Проходя через множество полок ("тарелок") ректификационной колонны, пар успевает настолько обогатиться более летучим компонентом, что на выходе из колонны практически содержит только этот компонент (или азеотропную смесь).
Степень разделения зависит от того, насколько пар обедняется примесью по сравнению с жидкой фазой. Расчет показывает, что в современных лабораторных ректификационных колоннах высотой 1-2 м можно осуществить очистку в 10 5 раз и более, если даже содержание примеси в равновесном паре только на 10% меньше, чем в жидкости. Этим объясняется широкое использование дистилляции и ректификации в производстве чистых веществ.
Ректификация используется для очистки не только жидких препаратов. Общеизвестно применение ректификации для разделения сжиженных газов (кислород, азот, инертные газы и т. д.).
В последние годы с помощью ректификации стали очищать многие твердые вещества, сравнительно легко испаряющиеся. Удалось успешно очистить хлористый алюминий (от Fe), серу (от Se), SiCl 4 , Zn, Cd, SbСl 3 . Содержание примесей понижается до 10 -4 и даже до 10 -7 %. Таким образом, ректификация может быть отнесена к чрезвычайно эффективным методам глубокой очистки. Особенно эффективно протекают процессы ректификационной очистки при низких температурах; при повышении температуры резко возрастает загрязнение очищаемого вещества материалом аппаратуры.
Экстракция. Экстракционный метод разделения веществ применяют уже в течение многих десятилетий, особенно в аналитической химии, но только в последнее время он приобрел очень важное значение для получения чистых и сверхчистых веществ. Метод основан на извлечении одного из компонентов раствора с помощью несмешивающегося с раствором органического растворителя.
Достоинства экстракционного метода следующие:
экстракцию можно проводить из чрезвычайно разбавленных растворов (при достаточно большом коэффициенте распределения)
при экстрагировании не происходит соосаждения, и экстрагируемое вещество может быть количественно выделено в чистом виде
метод позволяет разделять такие вещества, которые не удается разделить иными методами, например, при очистке солей уранила от примесей Fe, В, Мо и др.
Зонная плавка. Этот метод очистки основан на различии растворимости примеси в твердом веществе и в расплаве. Образец твердого вещества медленно передвигают через узкую зону нагревания, при этом происходит постепенное расплавление отдельных участков образца, находящихся в данный момент в зоне нагревания. Примеси, содержащиеся в образце, накапливаются в жидкой фазе, вместе с ней передвигаются вдоль образца и по окончании плавки оказываются в конце образца. Как правило, зонную плавку повторяют многократно. Зачастую образец движется через несколько обогреваемых зон, что позволяет в несколько раз сократить время очистки.
Достоинствами зонной плавки являются простота аппаратурного оформления, сравнительно невысокие температуры проведения процесса (по сравнению с ректификацией) и высокая эффективность очистки. Таким путем, например, очищается германий до содержания примесей порядка 10 -8 %. С каждым годом все большее число веществ, предназначенных для самых ответственных целей, проходит очистку методом зонной плавки. С равным успехом можно очищать неорганические и органические продукты. Правда, зонная плавка не всегда может быть успешно использована. Например, зонной плавкой нельзя отделить Аu от Ag.
Документ... «Очистка загрязненной поваренной соли» Аннотация В дополнительном материале дана классификация основных методов разделения веществ ... и других точных отраслях промышленности. Для очистки веществ применяются различные способы разделения смесей...
Аннотация основной профессиональной образовательной программы по специальности спо 240705. 01 аппаратчик-оператор в биотехнологии
ДокументАннотация основной профессиональной образовательной... ним разрабатываются ФГАУ «ФИРО». Аннотации размещены согласно циклам дисциплин. Общепрофессиональные... и вредных веществ Тема 1.2.7 Условия хранения Тема 1.2.8 Инструкции по очистке и хранению...
Аннотация примерной программы учебной дисциплины «Экология» Цели и задачи дисциплины
ДокументЧасти цикла «Экология» Аннотация примерной программы учебной дисциплины « ... . Взаимодействие живого и биокостного вещества . Энергетический баланс биосферы. Биогеохимические... выбросов. Современные технологии очистки и снижение выбросов загрязняющих...