1597 0
Иммунный ответ возникает в результате воздействия чужеродного агента. Соединение, которое вызывает реакцию, относят или к антигенам, или к иммуногенам. Различие между ними заключается в их функциях. Антигеном является любой агент, способный специфически связываться с компонентами иммунного ответа, такими как рецепторы В-клеток (BCR) на В-лимфоцитах, и растворимыми антителами.
Иммуноген же представляет собой агент, способный вызывать иммунную реакцию и таким образом являться иммуногенным. Различать эти два термина необходимо, поскольку имеется много соединений, не способных вызывать иммунную реакцию и в то же время способных связываться с компонентами иммунной системы , которые были выработаны специально против них. Таким образом, все иммуногены являются антигенами, но не все антигены являются иммуногенами. Это различие становится очевидным в случае с соединениями низкой молекулярной массы, группой веществ, включающей многие лекарства и антибиотики.
Сами по себе эти соединения не способны вызвать иммунный ответ, но когда они объединяются с гораздо более крупными агентами, такими как протеины, формируется конъюгат, способный вызывать иммунный ответ, направленный против различных частей конъюгата, в том числе и его составляющую с низкой молекулярной массой.
Действующее таким образом низкомолекулярное вещество относится к гаптенам (от греч. hapto - схватывать), в то время как соединение с высокой молекулярной массой, с которым соединяется гаптен, называется носителем. Таким образом, гаптен является соединением, не способным самостоятельно вызывать иммунный ответ, но против которого иммунный ответ может быть получен путем иммунизации, если гаптен конъюгирован с носителем.
Иммунный ответ был получен против всех известных семейств биохимических соединений, таких как углеводы, липиды, протеины и нуклеиновые кислоты. Он может быть получен и к лекарствам, антибиотикам, пищевым добавкам, косметическим средствам, мелким синтетическим пептидам, но только в том случае, если они объединены с носителем. В этой главе будут обсуждаться основные свойства соединений, которые делают их антигенами и иммуногенами.
Для того чтобы обладать свойствами иммуногенности, соединение должно иметь следующие характеристики: 1) чужеродность; 2) большая молекулярная масса; 3) сложное химическое строение; 4) в большинстве случаев способность к разрушению (деградации) и взаимодействию с МНС организма-хозяина.
Чужеродность
Обычно у животных не отмечают аутоиммунных реакций. Так, если кролику, например, вводят его собственный сывороточный альбумин, он не вызовет иммунной реакции, поскольку распознается как собственный. Напротив, если сывороточный альбумин кролика вводят морской свинке, он будет распознаваться как чужеродный кроличий сывороточный альбумин и вызывать иммунный ответ.Чтобы доказать сохранность иммунитета у кролика, у которого не наблюдалось иммунной реакции на собственный сывороточный альбумин, ему можно ввести альбумин морской свинки. У кролика с сохраненным иммунитетом будет наблюдаться иммунная реакция на сывороточный альбумин морской свинки, поскольку эта субстанция будет определяться как чужеродная. Таким образом, первым требованием к веществу, рассматриваемому как иммуногенное, является чужеродность. Чем более чужеродным является вещество, тем более оно иммуногенно.
Обычно соединения, синтезируемые в организме хозяина, не являются для него иммуногенными. Однако имеются исключения, когда у индивидуума отмечается иммунная реакция на свои собственные ткани. Это состояние называется аутоиммунитетом.
Большая молекулярная масса
Вторым необходимым свойством иммуногена является определенная минимальная молекулярная масса вещества. Обычно соединения малой молекулярной массой менее 1 000 Да (например, пенициллин, прогестерон, аспирин) не являются иммуногенными. Соединения молекулярной массой между 1000 и 6000 Да (например, инсулин, адренокортикотропный гормон) могут быть иммуногенными, а могут и не быть. Соединения молекулярной массой более 6000 Да (например, альбумин, столбнячный токсин) обычно являются иммуногенными. Итак, относительно мелкие молекулы соединений обладают низкой иммуногенностью, в то время как большие - высокой.Сложная химическая структура
Третьим свойством, которым должно обладать соединение, чтобы быть иммуногенным, является определенный уровень физико-химической сложности. Например, простые молекулы, такие как гомополимеры аминокислот (например, полимер лизина молекулярной массой 30000 Да) редко являются хорошими иммуногенами. Аналогично, гомополимер поли-γ-D-глутаминовой кислоты (материал капсулы бациллы сибирской язвы) молекулярной массой 50000 Да не является иммуногенным.Рис. 3.1. Уровни организационной структуры протеина. На первичную структуру указывает линейное расположение аминокислот (для чего используют однобуквенный код); также отмечается наличие внутри цепи разных дисульфидных мостиков. Вторичная структура возникает при укладывании полипептидной цепи в α-спирали и β-складки. Третичная структура, показанная в виде ленточной диаграммы, формируется путем складывания участков вторичных структур (адаптировано с разрешения Р Sun, JC Boyington, Current Protocols in Protein Science, Wiley)
Отсутствие иммуногенности, несмотря на большую молекулярную массу этих веществ, обусловлено отсутствием достаточной химической сложности. Однако при увеличении химической сложности путем присоединения к ε-аминогруппе полилизина дополнительных частей, таких как динитрофенол, или других соединений с низкой молекулярной массой, не являющихся иммуногенными, такая макромолекула становится иммуногенной.
Получаемый иммунный ответ направлен не только против спаренных соединений с низкой молекулярной массой, но и против гомополимера с высокой молекулярной массой. Обычно увеличение химической сложности соединения сопровождается увеличением его иммуногенности. Так, сополимеры некоторых аминокислот, таких как полиглутаминовой, аланиновой и лизиновой (poly-GAT), обычно обладают высокой иммуногенностью.
Поскольку многие иммуногены являются протеинами, важно понять структурные свойства этих молекул. Каждый из четырех структурных уровней белка вносит свой вклад в появление иммуногенности у молекулы. При инициации приобретенного иммунного ответа распознаются многие структурные характеристики и химические свойства соединений.
Например, антитела могут распознавать такие структурные характеристики протеина, как первичная структура (последовательность аминокислот), вторичные (структуры каркаса полипептидной цепи, такие как α-спираль или (β-складка) и третичные структуры (сформированные трехмерной конфигурацией белка, которая создается при складывании полипептидной цепи и поддерживается дисульфидными мостиками, водородными связями, гидрофобными взаимодействиями и т.д.) (рис. 3.1). Могут распознаваться и четвертичные структуры (сформированные наложением отдельных частей, если молекула состоит из более чем одной субъединицы белка) (рис. 3.2).

Рис. 3.2. Четвертичная структура белков, возникающая из связи двух или более полипептидных цепей, которые формируют полимерный белок (адаптировано с разрешения Р Sun and JC Boyington, Current Protocols in Protein Science, Wiley)
Способность разрушаться
Для антигенов, активирующих Т-клетки, способность стимулировать иммунный ответ определяется возможностью взаимодействия с молекулами МНС, экпрессированными на антигенпрезентирующих клетках (АПК) . Последние должны вначале расщепить антиген, подвергнуть его ферментной деградации (этот процесс называется процессированием антигена), после чего антигенные эпитопы (небольшие фрагменты иммуногена) могут быть представлены на поверхности АПК. После деградации и возникновения нековалентной связи с МНС эти эпитопы стимулируют активацию и расширение клона антиген-специфичных эффекторных Т-клеток.Чувствительность протеинового антигена к ферментативной деградации во многом зависит от двух свойств: 1) он должен быть достаточно стабильным для того, чтобы попасть к месту взаимодействия В- или Т-лимфоцитов, что необходимо для развития иммунного ответа; 2) соединение должно относительно легко поддаваться частичной ферментативной деградации, которая происходит во время процессирования антигена антигенпрезентирующих клеткок.
Пептиды, состоящие из D-аминокислот, которые устойчивы к ферментативной деградации, не являются иммуногенными, в то время как их L-изомеры, чувствительные к ферментам, являются иммуногенными. Напротив, углеводы , которые не подвергаются изменениям и не презентируются, не могут активировать Т-клетки, хотя активируют В-клетки.
В целом, чтобы быть иммуногенным, вещество должно обладать всеми этими четырьмя свойствами. Оно должно быть чужеродным тому, кому введено, иметь относительно большую молекулярную массу, обладать определенной степенью химической сложности и быть способным к деградации.
Гаптены
Как указывалось ранее, вещества, называемые гаптенами, не вызывают иммунного ответа в своей первоначальной форме из-за низкой молекулярной массы и простоты химического строения. Эти соединения не иммуногенны до тех пор, пока они не соединятся с носителями, обладающими сложной химической структурой и высокой молекулярной массой. Таким образом, иммунный ответ может быть вызван тысячами химических соединений, как с высокой, так и с низкой молекулярной массой при условии, что они соединены с носителями, обладающими сложной химической структурой и высокой молекулярной массой.Другие условия появления иммуногенности
Существует также ряд других факторов, определяющих, будет ли вещество иммуногенным. Важную роль в том, будет ли данное вещество вызывать иммунную реакцию, играет генетическая организация (генотип) иммунизируемого индивидуума. Генетический контроль иммунной реактивности осуществляется в основном генами, картированными внутри МНС. Другой решающий фактор, определяющий иммуногенность веществ, - индивидуальный репертуар В- и Т-клеток.Реакции приобретенного иммунитета запускаются после связывания антигенных эпитопов с антигенспецифичными рецепторами на В- и Т-лимфоцитах. Если у индивидуума отсутствует определенный клон лимфоцитов, состоящий из клеток, несущих идентичный антигенспецифичный рецептор, необходимый для ответа на данный антигенный стимул, иммунного ответа на такой эпитоп не будет. И, наконец, такие важные на практике факторы, как доза и метод введения антигена, также играют роль в проявлении веществом иммуногенности.
Недостаточные дозы антигена могут не вызвать иммунный ответ в связи с тем, что они будут не способны в должной мере активировать лимфоциты или потому что данная доза делает реагирующие клетки неотвечающими. Последнее из перечисленных явлений вызывает состояние толерантности к данному антигену. Возможность индуцировать иммунный ответ определяется не только необходимостью введения порогового количества антигена, но и числом вводимых доз. Далее будет показано, что для получения сильного иммунного ответа необходимо повторно ввести антиген.
Наконец, на результат иммунизации может повлиять путь введения антигена, поскольку именно он определяет, какие органы и популяции клеток будут вовлечены в реакцию. Антигены, вводимые наиболее распространенным способом - подкожно, обычно вызывают наиболее сильный иммунный ответ. Это связано с тем, что их захват, процессирование и представление (презентация) эффекторным клеткам осуществляются клетками Лангерганса, находящимися в коже и являющимися одними из наиболее эффективных АПК. Реакции на подкожное введение антигенов проявляются в лимфатических узлах, куда происходит отток лимфы от места введения.
Антигены, введенные внутривенно, переносятся вначале в селезенку, где могут индуцировать иммунологическую неотвечаемость, или толерантность, или, если они представлены антигенпрезентирующими клетками, вызвать иммунный ответ. Антигены, поступающие через рот (гастроинтестинальный путь), вызывают локальный антительный ответ в границах собственной пластинки кишечника, но часто приводят к возникновению системной толерантности к антигену. Наконец, введение антигенов через респираторный тракт (интраназальный путь) нередко вызывает аллергические реакции.
Поскольку иммунные реакции зависят от множества межклеточных взаимодействий, на тип и выраженность иммунного ответа влияют клетки, заполняющие орган, в который антиген доставляется первоначально. Обязательные для проявления иммуногенности условия, перечисленные ранее, составляют часть тонкого механизма контроля, описанного в следующих главах, который, с одной стороны, запускает приобретенный иммунный ответ, а с другой, защищает индивидуум от реакции на вещества в тех случаях, когда такие реакции являются вредными
Р.Койко, Д.Саншайн, Э.Бенджамини
Иммуногенность антигена - это способность в организме иммунизированного животного образования антител. Иммуногенность как биологическое свойство антигена является более сложным, чем антигенность. Антигенности того или иного вещества недостаточно, чтобы вызвать образование антител. В качестве примера можно привести гаптены, которые приобретают иммуногенность только после конъюгирования с соответствующим носителем.
Иммуногенность веществ сильно зависит от их молекулярной массы: чем выше молекулярная масса, тем выше иммуногенность. Отсюда вытекает важное практическое следствие - сшивка биополимеров между собой и другими белками повышает иммуногенность. Зависимость иммуногенности от молекулярной массы, по-видимому, определяется следующими причинами: во-первых, увеличение времени пребывания антигена в организме при возрастании его молекулярной массы; во-вторых, у высокомолекулярных антигеноа существенно возрастает способность взаимодействовать с макрофагами, в-третьих, с увеличением молекулярной массы в антигене увеличивается как общее количество антигенных детерминант, так и их разнообразие, что повышает эффективность взаимодействия] антигенов как с B-, так и с T-лимфоцитами.
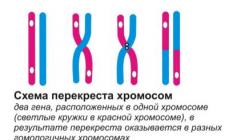
Плотность расположения и количество антигенных детерминант на поверхности антигенов также имеет важное значение: по мере увеличения этих показателей иммуногенность в начале растет, а затем начинает уменьшаться. Так, например, для динитрофенильной гаптеновой группы было показано, что из конъюгатов, содержащих 3, 16 и 28 групп на молекулу бычьего альбумина, максимальной антигенностью обладал конъюгат, содержащий 16 молекул гаптена. Одной из причин такого эффекта, по-видимому, является сложность межклеточной кооперации. В частности, показано, что в иммунном ответе против антигенов, имеющих повторяющиеся антигенные детерминанты, участвуют только В-лимфоциты; такие антигены называются независимыми . Для этих антигенов, например полимеров. D-аминокислот, также характерно снижение скорости метаболизма в организме.
Очень важным является понятие "чужеродность" иммуногена. Установлено, что чем более антиген отличается по своей структуре от гомологичного антигена иммунизируемого животного, тем выше его иммуногенность. Например, инсулины человека и многих видов животных имеют близкую первичную структуру и поэтому для них инсулин человека малоиммуногенен. Однако между инсулином человека и морской свинки имеются достаточные отличия, что позволяет использовать этих животных как продуцентов соответствующих антисывороток. Однако это правило нельзя считать абсолютным. Так, например, гормон тироксин имеет одинаковую структуру у всех животных, тем не менее, будучи конъюгированным с подходящим белком, он становится хорошим иммуногеном. В данном случае антигенная детерминанта состоит не только из гормона, но и "ножки" и части белковой глобулы, что в целом создает "чужеродную" структуру. Именно на этом принципе основано получение антител против различных низкомолекулярных физиологически активных веществ.
"Чужеродность" зависит от генетических особенностей иммунизируемого животного, поэтому часто иммуногенность связывают с генетической чужеродностью антигена. Из "чужеродности" следует, что иммуногенность - это не абсолютное свойство антигена по отношению к данному виду животного, а иногда даже к индивидуальному организму. Необходимо иметь в виду, что иммунная система организма сама находится под жестким генетическим контролем, который определяет как биологическую активность различных участников иммунного процесса, так и многообразие специфичностей рецепторов, а значит, и специфичностей антител. Именно видовая и индивидуальная вариабельность организмов требует внимательного выбора вида животного. Чем менее " чужеродный" антиген, тем большее количество животных следует брать для иммунизации. Так, например, для получения антисывороток против инсулина наиболее иммунореактивными являются морские свинки, при этом в среднем только одна из семи морских свинок дает удовлетворительную для целей анализа антисыворотку. Даже в случае получения антисывороток против достаточно "чужеродных" антигенов необходима большая группа животных, так как в этом случае нивелируются индивидуальные различия. Смесь антисывороток против данного антигена от разных животных одной группы называют пулом.
Из лабораторных животных чаще всего берут для иммунизации кроликов, морских свинок или мышей в зависимости от количества имеющегося антигена, доступности животного и т.д. Возможность использования группы лабораторных животных позволяет решить проблему отбора из них наиболее иммунореактивных. Иммунизировать удобнее самцов, так как у них иммуногенный ответ менее подвержен влиянию гормональных циклов. Для получения антител против вирусов эффективными оказались куры, у которых антитела накапливаются в яйцах. Большие количества антисывороток получают иммунизацией крупных животных: козлов, баранов, ослов, лошадей.
Для получения специфических антисывороток важное значение имеет гомогенность антигена. Это обусловлено тем, что примеси чужеродных антигенов могут обладать большей иммуногенностью, чем основной антиген, в результате чего, несмотря на небольшое количество примеси, против нее может образоваться достаточное количество антител. Так, например, вирусные антигены, выделенные из культуры ткани животных, содержат примесь тканевых антигенов, против которых вырабатываются антитела, дающие ложноположительные реакции в иммунохимическом анализе.
Степень иммунного ответа также зависит от количества введенного антигена. При определенных концентрациях антигена, как высоких, так и низких, наступает торможение гуморального иммунного ответа, называемое толерантностью. Это обусловливает необходимость выбора оптимальной дозы в каждом конкретном случае, с учетом чистоты препарата и его иммуногенности. Доза иммуногена для одной инъекции кролику или морской свинке составляет в среднем 100-300 мкг на 2 кг массы. Доза, необходимая для крупных животных, не увеличивается пропорционально их массе. Так, для овец достаточна доза, равная 0,25-5 мг иммуногена на инъекцию, для осла - 0,5-10 мг. В случае использования в качестве иммуногена конъюгата гаптенноситель доза зависит от молекулярной массы конъюгата.
Способ введения антигена и периодичность введения влияют на иммунологическую активность антисывороток. Так как иммунный ответ формируется в организме постепенно, принято различать первичный ответ и вторичный ответ . Первичные и вторичные антисыворотки отличаются по составу антител и их специфичности. Обычно высокоактивные антисыворотки получают после нескольких циклов иммунизации. Однако очень длительные иммунизации могут привести к снижению специфичности из-за постепенного увеличения титра антител к примесным антигенам.
В процессе иммунизации изменяется также аффинность и соотношение между различными фракциями антител. Такая вариабельность качества антисывороток по специфичности антител, их физико-химическим свойствам и концентрации является следствием популяционной природы иммунного ответа. В связи с этими обстоятельствами на практике необходимо вести непрерывный контроль за качеством получаемых антисывороток.
Антиген – это биополимер органической природы, генетически чужеродный для макроорганизма, который при попадании в последний распознаётся его иммунной системой и вызывает иммунные реакции, направленные на его устранение.
Антигены обладают рядом характерных свойств: антигенностью, специфичностью и иммуногенностью.
Антигенность . Под антигенностью понимают потенциальную способность молекулы антигена активировать компоненты иммунной системы и специфически взаимодействовать с факторами иммунитета (антитела, клон эффекторных лимфоцитов). Иными словами, антиген должен выступать специфическим раздражителем по отношению к иммунокомпетентным клеткам. При этом взаимодействие компоненты иммунной системы происходит не со всей молекулой одновременно, а только с ее небольшим участком, который получил название «антигенная детерминанта», или «эпитоп».
Чужеродность является обязательным условием для реализации антигенности. По этому критерию система приобретенного иммунитета дифференцирует потенциально опасные объекты биологического мира, синтезированные с чужеродной генетической матрицы. Понятие «чужеродность» относительное, так как имму-нокомпетентные клетки не способны напрямую анализировать чужеродный генетический код. Они воспринимают лишь опосредованную информацию, которая, как в зеркале, отражена в молекулярной структуре вещества.
Иммуногенность - потенциальная способность антигена вызывать по отношению к себе в макроорганизме специфическую защитную реакцию. Степень иммуногенности зависит от ряда факторов, которые можно объединить в три группы: 1. Молекулярные особенности антигена; 2. Клиренс антигена в организме; 3. Реактивность макроорганизма.
К первой группе факторов отнесены природа, химический состав, молекулярный вес, структура и некоторые другие характеристики.
Иммуногенность в значительной степени зависит от природы антигена. Важна также оптическая изомерия аминокислот, составляющих молекулу белка. Большое значение имеет размер и молекулярная масса антигена. На степень иммуногенности также оказывает влияние пространственная структура антигена. Оказалась также существенной стерическая стабильность молекулы антигена. Еще одним важным условием иммуногенности является растворимость антигена.
Вторая группа факторов связана с динамикой поступления антигена в организм и его выведения. Так, хорошо известна зависимость иммуногенности антигена от способа его введения. На иммунный ответ влияет количество поступающего антигена: чем его больше, тем более выражен иммунный ответ.
Третья группа объединяет факторы , определяющие зависимость иммуногенности от состояния макроорганизма. В этой связи на первый план выступают наследственные факторы.
Специфичностью называют способность антигена индуцировать иммунный ответ к строго определенному эпитопу. Это свойство обусловлено особенностями формирования иммунного ответа - необходима комплементарность рецепторного аппарата иммунокомпетентных клеток к конкретной антигенной детерминанте. Поэтому специфичность антигена во многом определяется свойствами составляющих его эпитопов. Однако при этом следует учитывать условность границ эпитопов, их структурное разнообразие и гетерогенность клонов антигенреактивных лимфоцитовой специфичности. В результате этого организм на антигенное раздражение всегда отвечает поликлональными иммунным ответом.
Все вакцины, кроме генно-инженерных, гетерогенны по своему антигенному составу. При введении корпускулярных вакцин (живых или убитых) появляются продукты их распада, отличающиеся по физико-химическим свойствам. Образуются олигомеры, мономеры и низкомолекулярные фрагменты. Последние способны взаимодействовать со специфическими рецепторами иммуно- компонентных клеток, не вызывая иммунного ответа. Кроме того, очень крупные молекулы антигена с высокой степенью валентности также могут быть толерогенными. Менее гетерогенными являются анатоксины и высокоочищенные микробные фракции, используемые в качестве вакцин.
Иммуногенность полных антигенов, входящих в состав вакцин, зависит от размера и полимерности их молекул, иммуногенность гаптенов - от их эпитопной плотности на молекуле носителя. Низкополимерный антиген может вызывать не только слабый, но и качественно иной характер иммунного ответа по сравнению с высокополимерным антигеном.
С точки зрения молекулярной и клеточной иммунологии вакцина должна удовлетворять следующим требованиям:
- Вакцина должна активировать вспомогательные клетки (макрофаги, дендритные клетки, клетки Лангерганса), участвующие в процессинге и представлении антигена.
- Она должна содержать эпитопы для Т- и В-клеток, обеспечивающие необходимое соотношение гуморального и клеточного иммунитета.
- Она должна легко подвергаться процессированию, ее эпито- пы должны обладать способностью взаимодействовать с антигенами гистосовместимости 1 и/или II класса.
- Она должна индуцировать образование регуляторных клеток (Т-хелперов), эффекторных клеток (киллеров, Т-эффекторов ГЗТ, антителообразующих клеток) и клеток иммунологической памяти.
Идеальная вакцина должна соответствовать двум основным требованиям: она должна быть безопасной и высокоэффективной. Она должна вводиться один раз и обеспечивать пожизненный иммунитет у 100% привитых. Таких вакцин пока нет. Несмотря на большие успехи в области совершенствования существующих вакцин и разработки новых препаратов, длительность иммунитета, возникающего после введения большинства вакцин, мала даже при условии многоразового введения одной и той же вакцины. Для некоторых вакцин она составляет всего 1 год (табл. 25). Указанные в таблице данные получены разными авторами в разное время и являются достаточно условными. Следует отметить, что у иммунизированных лиц определенная степень специфической защиты остается и после исчезновения циркулирующих антител.
Таблица 25. Длительность иммунитета (по защитным титрам антител) после первичной иммунизации
|
Сила иммунного ответа зависит от двух основных факторов: свойств макроорганизма и особенностей антигенов, используемых для иммунизации. Иммуногенность антигенов, получаемых из возбудителей инфекционных болезней, неодинакова. Наиболее иммуногенны экзотоксины и поверхностные антигены микроорганизмов. Иммуногенность вакцины во многом зависит от того, насколько удачно выбраны антигены для конструирования препарата. При недостаточной его иммуногенности используют неспецифические иммуностимуляторы (адъюванты). В практике вакцинации в качестве иммуностимуляторов используют гидроокись алюминия, фосфат алюминия, фосфат кальция, полиоксидоний и белковые носители.
Трудности в создании высокоэффективных вакцин связаны также с особенностями макроорганизма, его генотипа, фенотипа, с существованием двух видов иммунитета (гуморального и клеточного), которые регулируются разными субпопуляциями клеток- хелперов (Тх1 и Тх2). Поствакцинальный иммунитет складывается из двух видов иммунных реакций: гуморального и клеточного. Отсутствие циркулирующих антител еще не является доказательством слабости иммунитета, при новой встрече с антигеном иммунный ответ развивается за счет иммунологической памяти. Кроме того, в основе резистентности к некоторым видам инфекций лежат клеточные механизмы, поэтому вакцины, используемые для профилактики этих инфекций, должны формировать клеточный иммунитет.
Иммуногенность вакцин составляет основу ее эффективности. Как правило, корпускулярность вакцин (живых, убитых) обеспечивает необходимую иммуногенность, в остальных случаях часто приходится использовать дополнительные методы повышения иммуногенности вакцин.
Способы повышения иммуногенности вакцин
- Использование оптимальной концентрации антигена.
- Очистка вакцин от низкомолекулярных веществ, способных вызывать специфическую или неспецифическую супрессию иммунного ответа.
- Агрегация антигена с помощью ковалентного связывания и других методов комплексообразования.
- Включение в вакцину максимального количества эпитопов антигена.
- Сорбция на веществах, создающих депо антигена (гидроокись алюминия, фосфат кальция и др.).
- Использование липосом (водно-масляной эмульсии).
- Добавление микробных, растительных, синтетических и других видов адъювантов.
- Связывание слабого антигена с белковым носителем (столбнячным, дифтерийным анатоксином и др.).
- Включение антигена в микрокапсулы, обеспечивающие выброс антигена через заданный промежуток времени.
10. Улучшение условий процессинга и представления антигена. Использование антигенов гистосовместимости 1 и II классов или антител к этим антигенам.
Подходы к созданию вакцин, обеспечивающих формирование клеточного и гуморального иммунитета, различны. Это обусловлено участием в иммунном ответе двух регуляторных клеток: Тх1 и Тх2. Между ними существует определенная степень антагонизма, хотя они и образуются из одного и того же вида клеток-предше- ственников. Получить вакцину, которая бы вызывала клеточный иммунитет, достаточно трудно. Во многих случаях не удается переключить иммунный ответ Тх2 на вакцину, которая стимулирует образование антител, на клеточный ответ Тх1.
Крайне важно, чтобы вакцины вызывали Т-зависимый иммунный ответ. В противном случае ответ будет кратковременным, а повторное введение вакцины не будет вызывать вторичный ответ. Первичный и вторичный иммунный ответ отличаются друг от друга по динамике формирования иммунитета (рис. 11). Вторичный иммунный ответ недостаточно выражен, если для иммунизации используется слабый антиген, если в организме присутствуют пассивно введенные или активно приобретенные антитела, если антиген вводят пациенту с иммунодефицитом.
Вторичный иммунный ответ характеризуются следующими признаками:
- Более раннее (по сравнению с первичным ответом) развитие иммунных реакций.
- Уменьшение дозы антигена, необходимой для достижения оптимального ответа.
- Увеличение силы и продолжительности иммунного ответа.
- Усиление гуморального иммунитета:
– увеличение количества антителообразующих клеток и циркулирующих антител;
– активация Тх2 и усиление выработки их цитокинов (ИЛ-3, 4, 5, 6, 9, 10, 13, ГМ-КСФ и др.);
– сокращение периода образования ^М-ангител, преобладание 1нСт- и IgA-aнтитeл;
– повышение аффинности антител.
5. Усиление клеточного иммунитета:
– увеличение числа антигенспецифических Т-киллеров и Т-эффекторов ГЗТ;
– активация Тх1 и усиление выработки их цитокинов (ИФ-у, ФИО, ИЛ-2, ГМ-КСФ и др.);
– повышение аффиннности антигенспецифических рецепторов Т-клеток.
6.Повышение устойчивости к заражению.
Способность быстро реагировать на повторный контакт с антигеном организм приобретает благодаря иммунологической памяти. Она характерна для клеточного и гуморального иммунитета, зависит от формирования Т- и В-клеток памяти. Иммунологическая память развивается после перенесенной инфекции или вакцинации и сохраняется длительное время.
При некоторых инфекциях антитела в сыворотке крови присутствуют на протяжении десятилетий. Вместе с тем полупериод жизни самого устойчивого иммуноглобулина составляет в среднем 25 дней. Таким образом, в организме постоянно происходит ре- синтез специфического иммуноглобулина.
Длительность постинфекционного иммунитета зависит от свойств возбудителя, инфицирующей дозы, состояния иммунной системы, генотипа, возраста и других факторов. Иммунитет может быть кратковременным, например при гриппе, дизентерии, возвратном тифе, достаточно продолжительным, например при сибирской язве, риккетсиозе, лептоспирозе, и даже пожизненным, например при полиомиелите, кори, коклюше.
Приобретенный иммунитет является хорошей защитой против заражения тем же возбудителем. Если основным механизмом иммунитета при данной инфекции является эффект нейтрализации, то наличие определенного уровня циркулирующих антител достаточно для предупреждения реинфекции.
Для достижения стойкого иммунитета вакцины приходится вводить 2 раза и более. Первичная вакцинация может состоять из нескольких доз вакцины, интервалы между дозами строго регламентированы. График проведения ревакцинации более свободный, ревакцинацию можно проводить через год и даже через несколько лет.
Интервал между введениями вакцины должен быть не менее 4 нед. В противном случае развивается менее стойкий иммунитет. Наоборот, некоторое увеличение 4-недельного интервала может усилить вторичный иммунный ответ. Максимальное повышение концентрации антител при вторичном ответе на вакцины возникает при невысоких исходных титрах антител. Высокий предшествующий уровень антител препятствует дополнительной выработке антител и длительному их сохранению, а в некоторых случаях наблюдается снижение титров антител.
Все вакцины, кроме генно-инжерных, гетерогенны по своему составу. Они содержат антигены разного размера и разной полимерности. Даже при введении корпускулярных вакцин (живых или убитых) появляются продукты их распада, отличающиеся по физико-химическим свойствам.
Образуются олигомеры, мономеры и низкомолекулярные фрагменты. Последние способны взаимодействовать со специфическими рецепторами иммунокомпетентных клеток, не вызывая иммунного ответа. Кроме того, очень крупные молекулы антигена с высокой степенью валентности также являются толерогенами.
Иммуногенность полных антигенов, входящих в состав вакцин, зависит от размера и полимерности их молекул, иммуногенность гаптенов - от их эпитоп- ной плотности на молекуле носителя. Низкополимерный антиген может вызывать не только слабый, но и качественно иной характер иммунного ответа по сравнению с высокополимерным антигеном. Прямая корреляция между иммуногенностью и полимерностью антигена имеет определенный предел, выше которого антиген приобретает толерогенные свойства. Это особенно характерно для полисахаридных антигенов. Для белков свойственна толерантность, вызванная низкополимерными антигенами.
С точки зрения молекулярной и клеточной иммунологии вакцина должна удовлетворять следующим требованиям:
1. Вакцина должна активировать вспомогательные клетки (макрофаги, дендритные клетки, клетки Лангерганса), участвующие в процессинге и презентации антигена.
2. Она должна содержать эпитопы для Т- и В-клеток, обеспечивающие необходимое соотношение гуморального и клеточного иммунитета.
3. Она должна легко подвергаться процессированию, ее эпитопы должны обладать способностью взаимодействовать с антигенами гистосовместимости класса I и (или) II.
4. Она должна индуцировать образование регуляторных клеток (Т-хелперов), эффекторных клеток (киллеров, Т-эффекторов ГЗТ, антителообразующих клеток) и клеток иммунологической памяти.
Идеальная вакцина должна удовлетворять двум основным требованиям: она должна быть безопасной и высоко эффективной. Она должна вводиться один раз и обеспечивать пожизненный иммунитет у 100% привитых. Таких вакцин пока нет. Несмотря на большие успехи в области совершенствования существующих вакцин и разработки новых препаратов длительность иммунитета, возникающего после введения большинства вакцин, мала даже при условии многоразового введения одной и той же вакцины. Для некоторых вакцин она составляет всего 1 год (табл. 25). Указанные в таблице данные получены разными авторами в разное время и являются достаточно условными.
| Вакцина | Годы |
| Коклюшная | 3 |
| Дифтерийный анатоксин | 7-10 |
| Столбнячный анатоксин | 1-5 |
| Против гепатита В | 5 |
| Коревая | 15 |
| Против краснухи | 20 |
| Против эпидемического паротита | 8 |
| Живая полиомиелитная | пожизненно |
| БЦЖ | 7-10 |
| Против гепатита А | 4 |
| Брюшнотифозная полисахаридная | 2 |
| Антирабическая | 3 |
| Против клещевого энцефалита | 3 |
| Менингококковая полисахаридная | 2 |
| Холерная | 6 мес |
| Против чумы | 1 |
| Против сибирской язвы | 1 |
| Против туляримии | 5 |
| Бруцеллезная | 1-2 |
| Против гемофильной Ь инфекции | 4 |
Сила иммунного ответа зависит от двух основных факторов: от свойств макроорганизма и особенностей антигенов, используемых для иммунизации.
Иммуногенность антигенов, получаемых из возбудителей инфекционных болезней, неодинакова. Наиболее иммуногенны экзотоксины и поверхностные антигены микроорганизмов. Иммуногенность вакцины во многом зависит, насколько удачны выбраны антигены для конструирования препарата. При недостаточной его иммуногенности используют неспецифические иммуностимуляторы (адъюванты). Их много, механизмы их действия разнообразны. Одни из них направлены на изменение свойств антигена, другие - на стимуляцию функций иммунной системы организма. В конечном счете иммуностимуляция связана с активированием иммунокомпетентных клеток, усилением их пролиферации и дифференцировки. В практике вакцинации в качестве иммуностимуляторов используют гидроокись алюминия, фосфат алюминия, фосфат кальция. В состав вакцины против гемофильной палочки входит белковый носитель
(столбнячный анатоксин), а в состав вакцины гриппол - синтетический стимулятор полиоксидоний.
Трудности в создании высокоэффективных вакцин связаны также с особенностями макрорганизма, его генотипа, фенотипа, с существованием двух видов иммунитета (гуморального и клеточного), которые регулируются разными субпопуляциями клеток-хелперов (Тх1 и Тх2). Поствакцинальный иммунитет складывается из двух видов иммунных реакций: гуморальной и клеточной. Отсутствие циркулирующих антител еще не является доказательством слабого иммунитета. В основе резистентности к некоторым видам инфекций лежат клеточные механизмы, поэтому вакцины, используемые для профилактики этих инфекций, должны формировать клеточный иммунитет.
Иммуногенность вакцин составляет основу ее эффективности. Как правило, корпускулярность вакцин (живых, убитых) обеспечивает необходимую иммуногенность, в остальных случаях часто приходится использовать дополнительные методы повышения иммуногенности вакцин.
Способы повышения иммуногенности вакцин
1. Использование оптимальной концентрации антигена.
2. Очистка вакцин от низкомолекулярных веществ, способных вызывать специфическую или неспецифическую супрессию иммунного ответа.
3. Агрегация антигена с помощью ковалентного связывания и других методов комплексообразования.
4. Включение в вакцину максимального количества эпитопов антигена.
5. Сорбция на веществах, создающих депо антигена (гидроокись алюминия, фосфат кальция и пр.).
6. Использование липосом (водно-масляной эмульсии).
7. Добавка микробных, растительных и других видов адъювантов.
8. Связывание слабого антигена с носителем (столбнячным, дифтерийным анатоксинами и др.).
9. Усиление иммуногенных свойств вакцины с помощью искусственных носителей-адъювантов (полиоксидоний и др.).
10. Включение антигена в микрокапсулы, обладающие адъювантными свойствами и обеспечивающие выброс антигена через заданный промежуток времени.
11. Улучшение условий процессинга и презентации антигена. Использование антигенов гистосовместимости класса I и II или антител к этим антигенам.